ヒトの体内において、細胞のバリアは多くの表層を形成し、組織を保護したり体内への物質の出入りをコントロールしています。これらの細胞バリアは、主に内皮細胞と上皮細胞で構成されており、バリアの浸透機能は、炎症、感染症、がん細胞の転移、白血球遊走などの生物学的事象によって改変されます。
Axion BioSystems の Maestro では、インピーダンス変化の検出により、細胞の変化をラベルフリーで連続して、測定・解析することが可能です。数日間に渡るバリアの破綻を連続して追跡することが可能です。
生体バリア完全性評価
経上皮電気抵抗 (TEER) はバリア機能の評価にしばしば用いられます。
Maestroによるインピーダンスアッセイは、経上皮電気抵抗値を測定し、バリアインデックスとして指標化します。Maestroは、複数の周波数条件でインピーダンスを測定します。低周波下で得られるインピーダンス値を、細胞の電極への被覆を示唆する高周波下のインピーダンス値でノーマライズすることにより、微細なバリア機能の変化を捉えます。
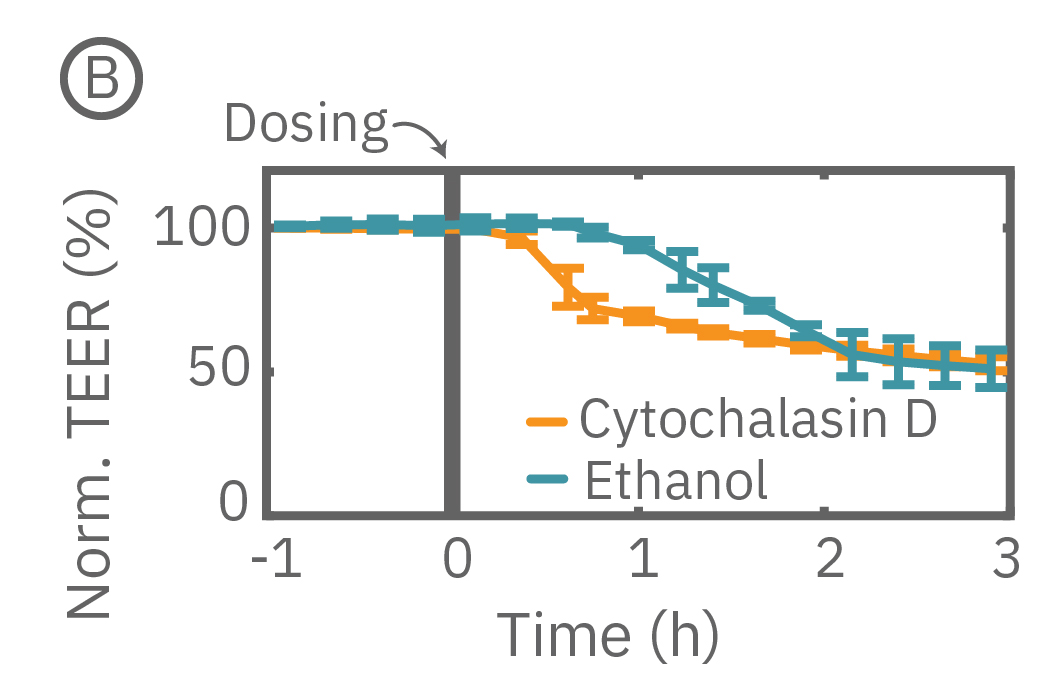
バリアの浸透機能は、一般的な薬剤や分子によっても改変されることがあります。本事例では、96 well フォーマットの CytoView-Z プレート上に Calu-3 細胞を播種し、Maestro Z で14日間に渡り連続してTEERを測定しました。細胞がプレート上でコンフル状態になった後、サイトカラシンD、エタノールをそれぞれ投与しました。サイトカラシンDは、アクチン重合を阻害し、タイトジャンクションの漏洩を増加させますが、この現象が急激なTEERの減少(B図オレンジ色)にて示されました。一方、エタノールは、タイトジャンクションにおける2種類の重要なたんぱく質であるZO-1とクローディン1結合に比較的ゆっくり影響を及ばしますが、この現象が緩慢なインピーダンスの減少によって示されました(B図水色)。
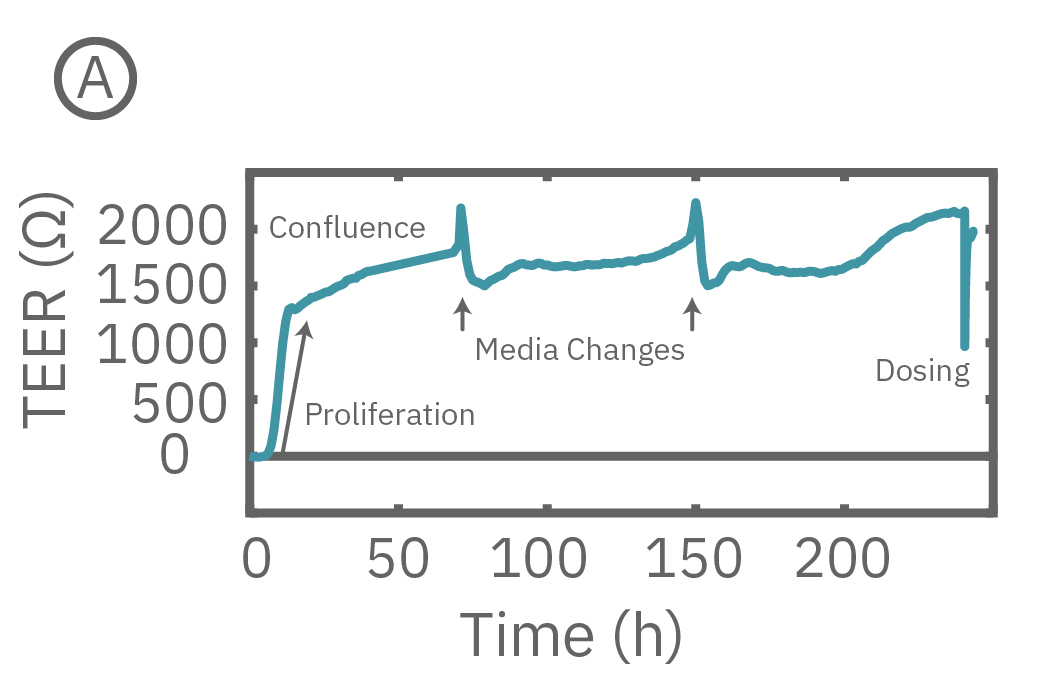
(A) CytoView-Z プレート上に Calu-3 細胞を播種し14日間に渡り連続してTEERを測定した。
(B) 14日後にサイトカラシンD (オレンジ色)とエタノール(水色)をプレート上の異なる well に投与したところ、TEERの減少が得られた。
Disease-in-a-dish モデルでのバリア機能評価
バリア機能はヒトの体内において重要な役割を担っていますが、嚢胞性線維症 などの病気により破壊することもあります。Calu-3細胞株は、不死化細胞であり、タイトジャンクションを形成します。また、嚢胞性線維症膜コンダクタンス制御因子 (CFTR) を発現させ、βアドレナリン性の刺激によりイオンを透過させます [Shen et al., 1994]。本事例では、TEER アッセイによりCFTRのこれらの機能を検証しています。
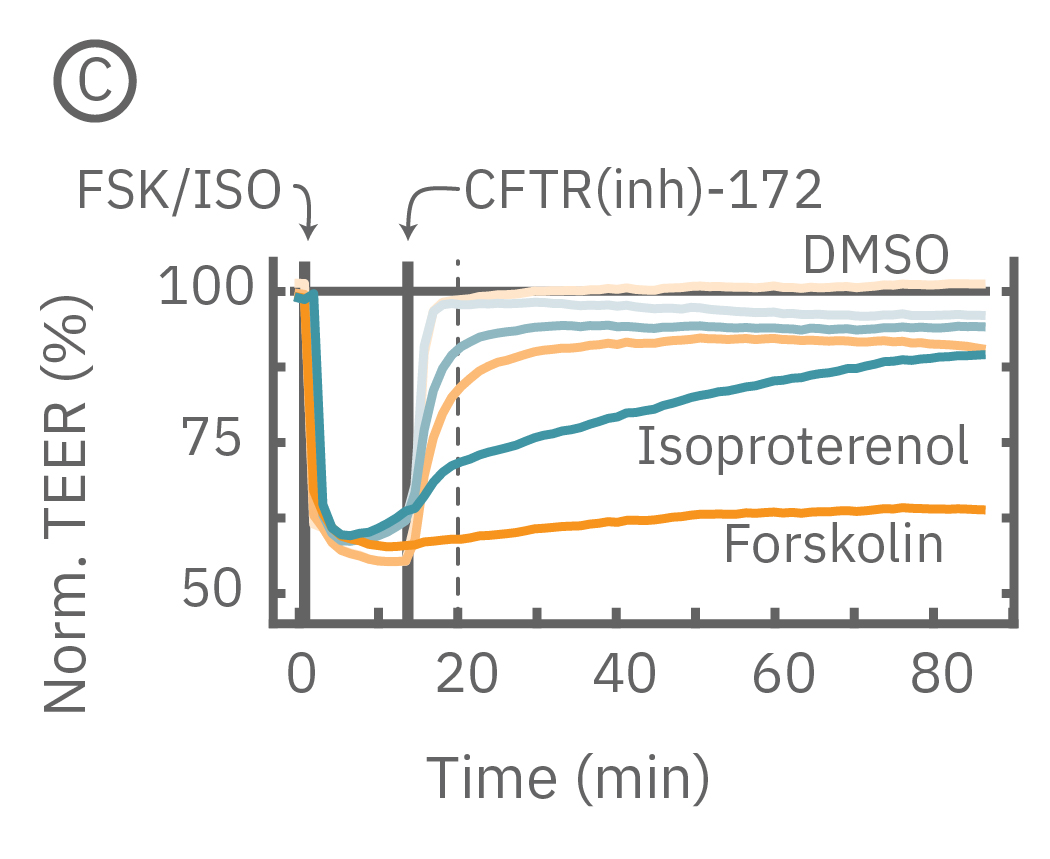
(C) プレート上で培養されたCalu-3細胞に、イソプレテレノール (水色、100 μM)とフォルスコリン (オレンジ色、10 μM)を投与したところ、TEERが急激に減少した。続いてCFTR(inh)-172を30 μM 及び300 μM の濃度で添加したところ、TEERに回復がみられその上昇は濃度に依存した。
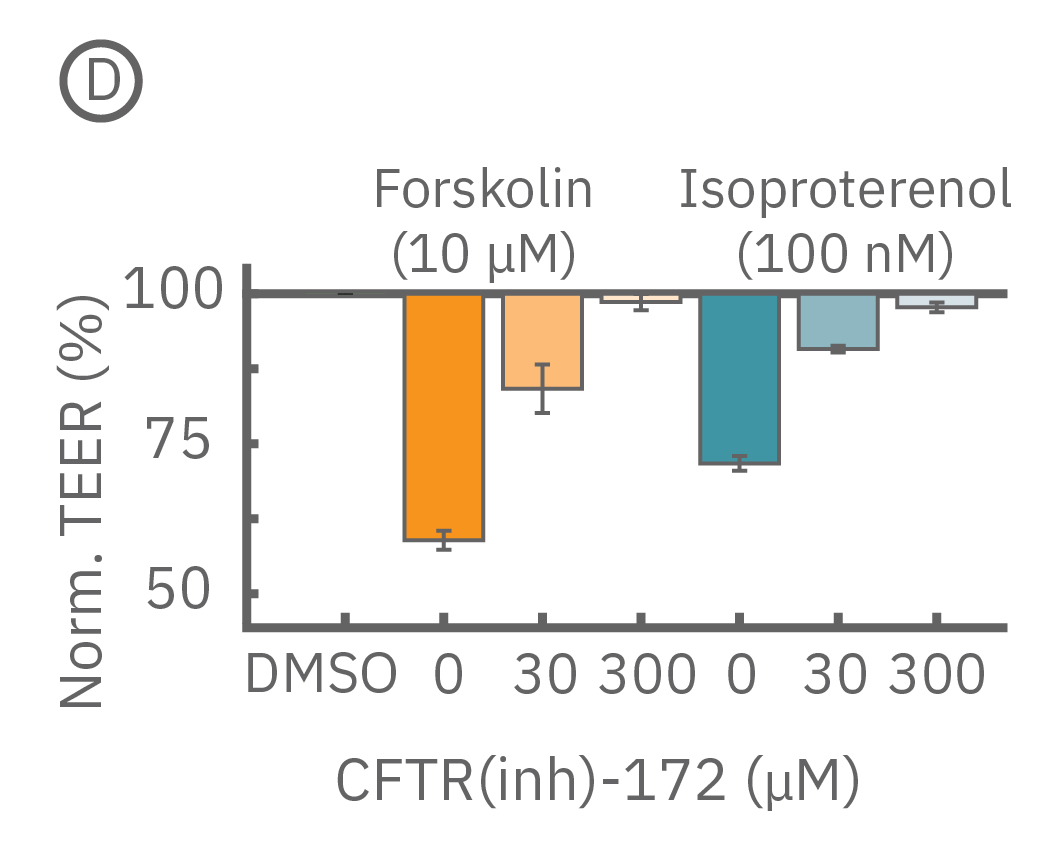
(D) CFTR(inh)-172投与から5分後 (C図点線箇所) のTEER。フォルスコリン、イソプレテレノール共に、CFTR(inh)-172による抑制反応は、濃度に依存した。
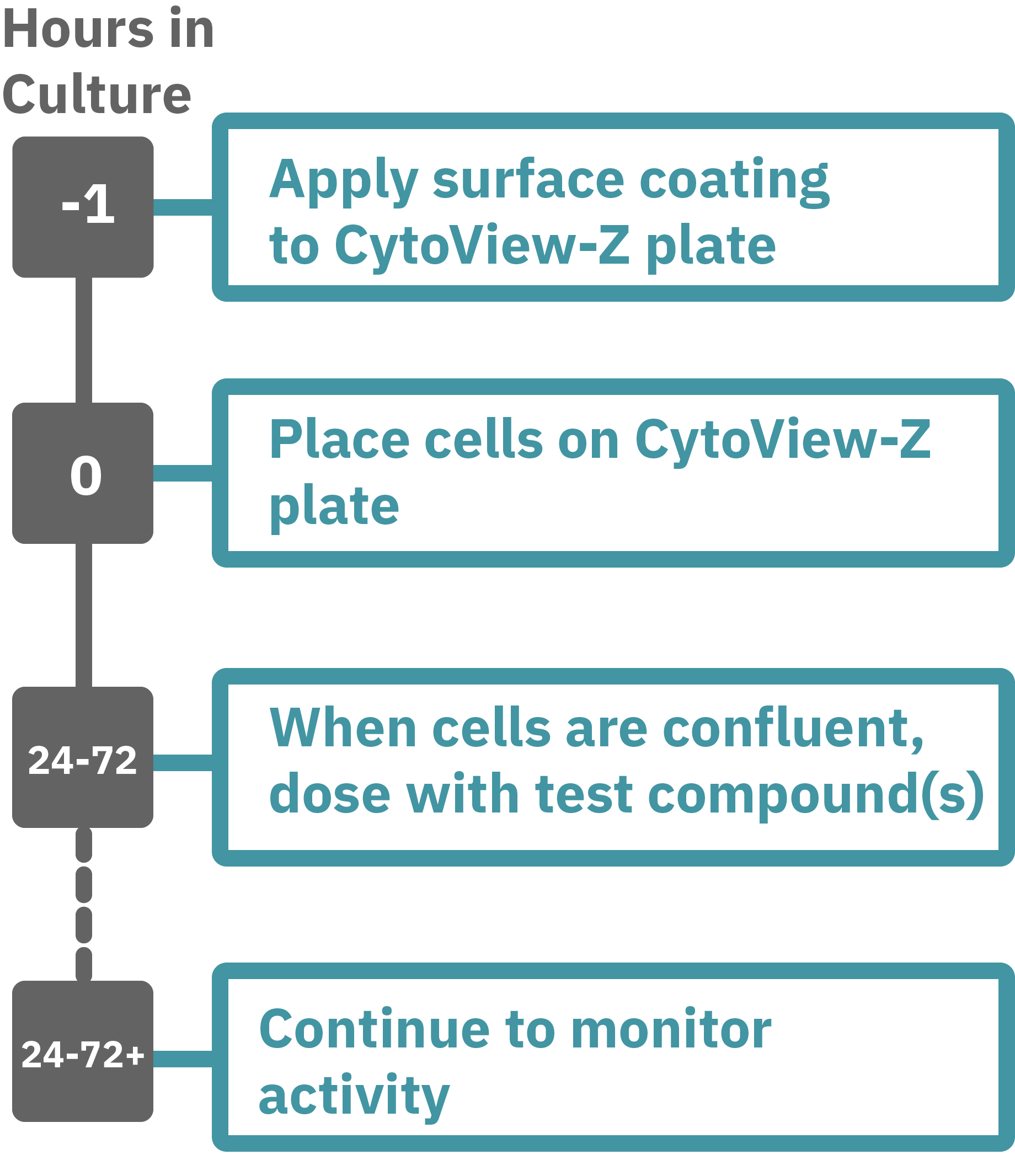
Maestroによる、バリア機能評価はとても簡単です。事前コーティングされた CytoView-Zプレート上に細胞を播種します (Hour 0)。Maestroシステムにプレートを搭載すると同時に、温度・CO₂ 濃度制御とインピーダンス測定が開始されます。細胞の増殖・電極への接着に伴いインピーダンスが上昇します (Hour 0 ~ 24-72)。
細胞がコンフルな状態なったら化合物などを投与し、以降数日間に渡って生体バリアの変化をラベルフリーで測定します。

Maestro Z/ ZHT, Pro/EdgeによるTEERアッセイ:特徴
-
経時的観察 - 96或いは384 well 同時に測定します。細胞バリア、タイトジャンクションの変化を連続して測定し、専用アプリで、実験室の外からでもライブデータの確認が可能です。
-
ラベルフリー - 平面電極によるインピーダンス測定は、染色・試薬などを必要としません。ラベルフリー測定で数日間に渡る測定・観察が可能です。
-
インキュベータ不要 - Maestro には温度・CO2濃度コントローラが内蔵されています。インキュベータ等の周辺装置は不要。安定した環境下で数日間に渡る連続測定が可能です。
-
細胞可視 - CytoView-Z 96 well プレート底面中央部は透明になっています。必要に応じて、細胞の観察が可能です。
-
培養から測定まで同一プレート使用 - アッセイの全行程を同一プレートで行います。他のハイスループット・プラットフォーム(例:フローサイトメータ)のような容器の入れ替えなどは不要。細胞への負担を最小限に抑えることができます。
-
スマートフォン・アプリ - 専用のスマートフォンアプリに対応しています。数日間に渡るバリアの変化の様子を、実験室の外からでも、リアルタイムに観察して頂けます。
-
簡単 - セミ・オートメーションシステムです。ハードウエアの操作はボタン1つ。専用のソフトは、インピーダンスの変化をリアルタイムで表示します。解析結果のエクスポートも容易です。

TEER
Show Full DetailsWhat is TEER-Based Barrier Analysis?
Trans-epithelial/endothelial electrical resistance (TEER) is a functional measure of barrier integrity across epithelial or endothelial cell layers. TEER assays quantify how effectively a cell monolayer restricts ion flow, providing a direct readout of tight junction formation and permeability. Maestro Z enables continuous TEER monitoring in multiwell plates, allowing researchers to track barrier development and disruption in real time.
Why Does Real-Time Barrier Monitoring Matter?
Barrier tissues play essential roles throughout the body, including in the lung, gut, vasculature, and blood–brain barrier. Disruption of barrier integrity is a hallmark of inflammation, infection, drug-induced toxicity, and disease. Traditional TEER methods are often low-throughput and manual, limiting kinetic insight. Maestro Z overcomes these limitations by delivering automated, hands-free TEER measurements across 96 wells simultaneously.

Impedance
Show Full DetailsWhat is impedance-based cellular analysis?
Impedance-based cell analysis is a label-free, real-time technology that monitors live cells by measuring how electrical signals change across microelectrodes embedded in the culture surface. As cells attach, spread, and respond to treatments, the Axion BioSystems' Maestro Z impedance platform provides dynamic, continuous cellular profiles — capturing both baseline behavior and drug- or immune-driven effects.
Why does real-time, label-free monitoring matter?
Traditional assays often rely on dyes, labels, or destructive endpoint measurements, which can interrupt normal biology and miss transient responses. Impedance monitoring solves this by delivering continuous, noninvasive functional readouts — enabling researchers to observe biological change as it happens, particularly in drug discovery, toxicology, and disease modeling.